حل كتاب النشاط علوم صف ثامن فصل ثاني
الطاقة الحرارية ودرجة الحرارة والحرارة
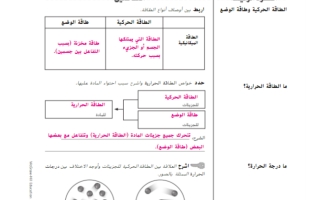
اربط بين أوصاف أنواع الطاقة
| الطاقة الحركية | طاقة الوضع | |
| الطاقة الميكانيكية | الطاقة التي يمتلكها الجسم أو الجزيء بسبب حركته | طاقة مخزنة بسبب التفاعل بين جسمين |
حدد خواص الطاقة الحرارية واشرح سبب احتواء المادة عليها
الطاقة الحركية :للجزئيات
طاقة الوضع : للجزيئات
الطاقة الحرارية : للمادة
الشرح : تتحرك جميع جزئيات المادة (الطاقة الحرارية ) وتتفاعل مع بعضها البعض ( طاقة الوضع)
اشرح العلاقة بين الطاقة الحركية للجزيئات وأوجه الاختلاف بين درجات الحرارة الممثلة بالصور
تتحرك جزيئات في B أسرع من الجزيئات في A ونظراً لأن الجزيئات في B تتحرك بشكل أسرع فإن لديها طاقة حركية أكبر وتعني زيادة متوسط الطاقة الحركية أن B تتمتع بدرجة حرارة أعلى
انتقالات الطاقة الحرارية
حدد 3 طرق تنتقل بها الطاقة الحرارية
1- الإشعاع
2- التوصيل
3- الحمل الحراري
حدد خواص الإشعاع
الإشعاع
انتقال الطاقة الحرارية بواسطة الأمواج الكهرومغناطيسية
يمكن أن يحدث من خلال
المواد الصلبة
السوائل
الغازات
الفراغ
صف التوصيل
التوصيل :انتقال الطاقة الحرارية بواسطة الاصطدامات بين الجزيئات
يمكن أن يحدث في
المواد الصلبة
السوائل
الغازات
قارن بين التوصيل والحرارة النوعية لمواصلات الحرارة وعوازل الحرارة
| موصل الحرارة | عازل الحرارة | |
| سهولة التوصيل | سهل | غير سهل |
| الحرارة النوعية | أقل | أعلى |
| السبب | تتحرك الإلكترونات بسهولة | لا تتحرك الإلكترونات بسهولة |
صنف خصائص التمدد الحراري والانكماش الحراري
| الانكماش الحراري | التمدد الحراري |
التعريف : ارتفاع في حجم المادة عند ارتفاع درجة الحرارة التأثير في بالون الهواء الساخن الهواء داخل بالون يسخن ويتمدد ويخرج بعض الهواء من البالون مما يجعله أقل كثافة من الهواء المحيط ويرفع البالون | التعريف :انخفاض في حجم المادة عند انخفاض درجة الحرارة التأثير في بالون الهواء الساخن يبرد الهواء داخل البالون وينكمش : يندفع الهواء من خارج البالون لملء المساحة وتزداد كثافة البالون ويهبط البالون |
صف الحمل الحراري
الحمل الحراري : انتقال الطاقة الحرارية بواسطة حركة الجزيئات من جزء من مادة إلى جزء آخر
يحدث في السوائل
اشرح تيارات الحمل الجوية
الهواء الأكثر دفئا والأقل كثافة يقوم بتدفئة الهواء المحيط
يصبح أكثر كثافة و ينخفض
الهواء الأكثر برودة والأكثر كثافة يمتص الطاقة الحرارية
يصبح أقل كثافة ويرتفع
التحليل : اشرح كيف يحدث جميع العمليات الثلاث التي تنقل الطاقة الحرارية أثناء قيامك بتسخين الحساء على الموقد
اقبل جميع الأجابات المنطقية : الإجابات النموذجية : يسخن الموقد المقلاة من خلال التوصيل وتنقل تيارات الحمل الطاقة الحرارية في السائل كله من الحساء ويمكنني ان أشعر بالحرارة من خلال الإشعاع عند وضع يدي بالقرب من المقلاه
استخدام الطاقة الحرارية
أكمل مفهوم تحويل الطاقة الحرارية
يمكن تحويل الطاقة الحرارية إلى أشكال أخرى من الطاقة
الأجهزة التي تحول الطاقة
يمكنها أن تؤدي العديد من المهام المفيدة
الأشكال الأخرى من الطاقة يمكن تحويلها إلى الطاقة الحرارية
صف أجهزة التدفئة
قم بتحويل الطاقة الكهربائية إلى الطاقة الحرارية
أمثلة : مكواة التجعيد - ماكينة تحضير القهوة - مكواة الملابس
سلسل المفاهيم والخطوات حول وظيفة منظم الحرارة في نظام التدفئة المنزلية
1- يحتوي منظم الحرارة على لفة ثنائية المعدن
2- نوعا المعادن يتمددان وينكمشان بشكل مختلف خلال تتغير درجة الحرارة
3- الهواء الدافئ في الغرفة يجعل اللفات غير مجعدة قليلاً
4- مما يحرك المفتاح الذي بإغلاق الفرن
صف عمليات انتقال الطاقة الحرارية التي تحدث في وظيفة الثلاجة
| الخطوة في العملية | التأثير على الطاقة الحرارية |
| الطاقة الميكانيكية بالمكبس تعمل على حفظ المبرد | يزيد الانضعاط الطاقة الحرارية للمبرد |
| تكون الطاقة الحرارية للمبرد أكبر من الطاقة الحرارية للهواء المحيط | تنتقل الطاقة الحرارية من خلال المبرد إلى الهواء |
| يصبح المبرد سائلاً | يفقد المبرد طاقته الحرارية |
| يحول الموسع المبرد من الحالة السائلة إلى الغازية | يحتوي الغاز على قدر أقل من الطاقة الحرارية ومن ثم يبرد |
| يمر الغاز البارد عبر الانابيب في صندوق الثلاجة | يمتص غاز المبرد الطاقة الحرارية من داخل الثلاجة |
| يصبح الغاز أكثر دفئا | يصبح الطعام أكثر برودة |
رتب تحويلات الطاقة في المحرك الحراري لسيارة
الطاقة الكيميائية من الوقود
تتحول إلى طاقة حرارية أثناء الاحتراق
نحو 20% تتحول إلى طاقة ميكانيكية
التركيب : أحد الأجهزة بداخل منزلك أو بالقرب منه يعمل على تحويل الطاقة الكيميائية إلى طاقة حرارية ويحول منظم حرارة الثلاجة الطاقة الحرارية إلى ميكانيكية
الإلكترونات ومستويات الطاقة
صف خصائص الجدول الدوري
| الخاصية | الوصف |
| العدد الذري | عدد البروتونات في ذرة العنصر |
| الكتلة الذرية | متوسط كتلة جميع النظائر المختلفة للعنصر |
| الدورة | صف من العناصر |
| المجموعة | عمود من العناصر |
| الفلزات | العناصر المرتبة على الجانب الأيسر من الجدول الدروي باستثناء H |
| أشباه الفلزات | العناصر المرتبة في نمط خطوات السلم بين الفلزات واللافلزات |
| اللافلزات | العناصر المرتبة على الجانب الأيسر من الجدول الدروي بالأضافة إلى الهيدروجين |
صف المركبات
تتكون المركبات من ذرات اثنين أو أكثر من العناصر التي تترابط معا بواسطة روابط كيميائية
لخص العلاقة بين مستوى طاقة الإلكترون وموقعه في ذرة ضع دائرة حول الكلمة التي تجعل كل عبارة صحيحة
كلما اقترب من النواة كان مستوى طاقة الإلكترون أقل/ أعلى
كلما ابتعد من النواة كان مستوى طاقة الإلكترون أقل/ أعلى
حلل التفاصيل الخاصة بالإلكترونات التكافؤ
الأبعد عن النواة
الأضعف جذب من النواة
تدخل في الرابطة الكيميائية
معظم الطاقة
نفس العدد لجميع العناصر في مجموعة (فيما عدا الهيليوم )
رتب التسلسل خطوات رسم وتفسير رسم بياني لنقاط الإلكترونات
1- تحديد عدد المجموعة الخاص بالعنصر
2- تحديد عدد إلكترونات التكافؤ وهو نفسه رقم الآحاد في عدد المجموعة
3- وضع نقطة واحدة في المرة الواحدة على كل جانب من رمز العنصر شكل ثنائيات من النقاط حتى يتم استخدامها
4- تحديد الذرة على أنها ثابته إذا تم وضع جميع النقاط هي ثنائيات
5- عدد النقاط المفردة لتحدد عدد الروابط التي يمكن للذرة غير الثابته تشكيلها
اشرح لماذا تكون الغازات النبيلة مستقرة
جميع الغازات النبيلة باستثناء الهيليوم لديها ثمانية إلكترونات تكافؤ لذلك يتم وضع كل إلكترونات التكافؤ الخاصة بها في ثنائيات
التحليل : استخدم ما تعلمته في الدرس لشرح سبب ندرة وجود العناصر في صورتها النقية
الإجابات النموذجية : ذرات معظم العناصر غير ثابته لأن لديها إلكترونات تكافؤ مفردة لذلك لديها ميل قوي للرتابط مع ذرات أخرى وتشكيل مركبات مع أزواج إلكترونات مكتملة
المركبات والصيغ الكيميائية والروابط التساهمية
تذكر المعلومات حول العناصر والمركبات اقرأ كل عبارة وإذا كانت صحيحة فاكتب صح في العمود الأوسط وإذا كانت خاطئة فاكتب خطأ في العمود الأوسط وأعد كتابة الكلمات التي تحتها خط لجعل العبارة صحيحة
| العبارة | صواب أم خطأ | التصحيح |
| المركبات هي تركيبات كيميائية من العناصر | صح | |
| المركبات عادة ما يكون لها نفس خواص الروابط التي تشكلت منها | خطأ | نادرا العناصر |
| تشكل الذرات روابط من خلال مشاركة الخواص الفيزيائية | خطأ | إلكترونات تكافؤ |
حدد الرابطة التساهمية
رابطة كيميائية عندما تشارك ذرتان لا فلزيتان بزوج واحد او أكثر من إلكترونات التكافؤ
صف أنواع الراوابط التساهمية
| رابطة تساهمية | وصف تشارك إلكترون تكافؤ | التعليق على قوة الرابطة |
| مفردة | تشارك ذرتين 1 زوج من إلكترونات التكافؤ | أصعف من الروابط التساهمية |
| مزدوجة | تشارك ذرتين 2 زوج من إلكترونات التكافؤ | أقوى من الروابط التساهمية الأحادية |
| ثلاثية | تشارك ذرتين 3 زوج من إلكترونات التكافؤ | أقوى من الروابط التساهمية الثنائية |
حدد 4 خواص مشتركة للمركبات التساهمية
1- درجة انصهار منخفضة
2- درجة غليان منخفضة
3- موصلات رديئة للكهرباء أو الطاقة الحرارية
4- عادة ما يكون غاز أو سائل في درجة حرارة الغرفة
أكمل التشبيه
تعد الذرة بالنسبة للعنصر مثل الجزيء القطبي بالنسبة للمركب
اشرح لماذا يعد الماء جزيء قطبي
جزيئات الماء القطبية لأن الإلكترونات السلبية تنجذب بقوة أكبر إلى ذرة الأكسجين مما يترك شحنة موجبة قليلا بالقرب من ذرات الهيدروجين
فرق بين الجزيئات القطبية وغير القطبية فيما يتعلق بالإلكترونات المتشاركة
الجزيئات القطبية : تتشارك الإلكترونات بشكل غير متساو
الجزيئات غير القطبية :تتشارك الإلكترونات بشكل متساو
اربط بين عبارة المثيل يذوب في مثيله وقدرة المركبات على إذابة بعضها البعض
يمكن أن تذوب المركبات القطبية في مركبات قطبية أخرى ويمكن أن تذوب المركبات غير القطبية في مركبات غير قطبية أخرى ولكن لا تذوب المركبات القطبية وغير القطبية في بعضها البعض
عرف الصيغة الكيميائية
الصيغة الكيميائية هي مجموعة من الرموز والأعداد التي تمثل العناصر وعدد ذرات كل كل عنصر التي تكون المركب
اشرح الصيغة الكيميائية لجزيء من الماء صف ما يمثله كل رمز
يشير إلى الهيدروجين
يشير إلى ذرتين من الهيدروجين في كل جزئ من الماء
يشير إلى ذرة أكسجين واحدة
حدد أربعة أنواع من النماذج الجزيئية
رسم بياني للنقاط
الصيغة الثنائية
نموذج الكرات والعصي
نموذج ملء المساحة
اشرح لماذا توجد مركبات تساهمية اكثر بكثير من وجود عناصر نقية
هناك عدة تركيبات من الطرق الممكنة التي يمكن أن تتشارك بها إلكترونات التكافؤ وتميل الذرات غير الثابته إلى الترابط من أجل أن تصبح أكثر ثباتا
الروابط الأيونية والفلزية
نظم المعلومات الخاصة بالأيونات
تكتسب الذرة إلكترونا تصبح الشحنة الكلية سالبة
تفقد الذرة إلكترونا تصبح الشحنة الكلية موجبة
حلل ما يحدث لذرات الصوديوم والكلور في تشكيل كلوريد الصوديوم المركب
| الصوديوم | الكلور | |
| نوع العنصر | فلز | لا فلز |
| العدد الذري | 11 | 17 |
| عدد لإلكترونات التكافؤ | 1 | 7 |
| ثابته أم غير ثابته | غير ثابته | غير ثابته |
| انتقال الإلكترون | 1 مفقود | 1 مكتسب |
| الوصف بعد الانتقال | ثابت 10 إلكترونات مثل النيون | ثابت 18 إلكترونات مثل الأرجون |
| نوع الأيون | موجب | سالب |
حدد خمس خواص مشتركة للمركبات الأيونية
1- تنجذب الأيونات بقوة لبعضها البعض
2- موصلات جيدة للكهرباء عندما تكون في الماء
3- عادة ما تكون صلبة في درجة الحرارة الغرفة
4- درجة انصهار مرتفعة
5- درجة غليان مرتفعة
اشرح كيف تتكون الرابطة الفلزية
الرابطة الفلزية تتكون عندما تشارك العديد من ذرات الفلز بإلكترونات التكافؤ المجمعة لديها
صف ثلاثة خواص للمركبات الفلزية
درجتا انصهار وغليان مرتفعتان
موصلات جيدة للطاقة الحرارية والكهرباء
يمكن طرقها إلى ألواح او سحبها وتشكيلها في صورة أسلاك
قارن بين ثلاث طرق يمكن ان ترتبط الذرة من خلالها وتصبح ثابته
| العملية | تجميع الإلكترون | انتقال الإلكترون | تشارك الألكترون |
| نوع الرابطة الكيميائية | فلزية | أيونية | تساهمية |
| الوصف | لا ترتبط إلكترونات التكافؤ في ذرات الفلز بأي ذرة واحدة | لا تنتقل إلكترونات التكافؤ من الذرات اللافلزية إلى الذرات الفلزية | تتشارك إلكترونات التكافؤ بواسطة الذرات اللافلزية |
اشرح الفرق بين الذرة المحايدة والذرة الثابته
تكون الذرة ثابته إذا كان أعلى مستوى طاقة بها يحتوي على الحد الأقصى من عدد الإلكترونات المقترنة ثنائيا وتكون الذرة محايدة كهربائيا إذا كان لها نفس عدد البروتونات والإلكترونات التي تتوازن منها الشحنات الموجبة والسالبة
فهم التفاعلات الكيميائية
حدد الفرق بين التغير الفيزيائي والتغير الكيميائي
التغير الفيزيائي: لم يتم إنتاج مواد جديدة ولكن قد يكون للمواد الموجودة قبل وبعد التغير خواص فيزيائية مختلفة
التغير الكيميائي: تتغير مادة واحدة اة أكثر إلى مواد جديدة ذات خواص فيزيائية وكيميائية مختلفة
رتب بالتسلسل التغيرات في الذرات خلال التفاعل الكيميائي
تتفكك الروابط بين الذرات
إعادة ترتيب الذرات
تتشكل روابط كيميائية جديدة
وضح بالتفصيل المعلومات التي تتعلق بكتابة معادلات كيميائية
| حدد المادة المتفاعلة | المواد التي تبدأ في تفاعل كيميائي |
| حدد المنتج | المواد الناتجة عن تفاعل كيميائي |
| اكتب البنية العامة للمعادلة الكيميائية | المادة المتفاعلة +المادة المتفاعلة تعطي الناتج +الناتج |
| كيف تتم قراءة علامة السهم | بمعنى تنتج أو الناتج |
أعد ذكر نص قانون حفظ الكتلة
الكتلة الكلية قبل تفاعل كيميائي هي الكتلة الكلية نفسها بعده
اربط الذرات بالكتلة في تفاعل كيميائي
الكتلة قبل التفاعل الكيميائي مساويا ل الكتلة بعد التفاعل الكيميائي
عدد الذرات في المواد المتفاعلة مساويا ل عدد الذرات في الناتج
أعد صياغة ما تعنيه عندما تقول المعادلة الكيميائية متوازية
الأرقام المحددة لأنواع الذرات هي نفسها على كلا جانبي المعادلة
رتب الخطوات المستخدمة في موازنة المعادلة الكيميائية
1- اكتب المعادلة غير المتوازنة
2- عد ذرات كل عنصر في المواد المتفاعلة والناتج
3- أضف معاملات لتحقيق التوازن بين الذرات
4- اكتب المعادلة الكيميائية المتوازنة
أنواع التفاعلات الكيميائية
إجمالا مفهوم الأنماط في التفاعلات الكيميائية
انواع التفاعلات الكيميائية الرئيسية
عدد الأنواع 4
تم التحديد بواسطة طريقة إعادة تجميع الذرات
صف تفاعلات الاستبدال وقم بتضمين نموذج تفاعلات الاستبدال الأحادية والمزدوجة مع وصفك
تفاعلات الاستبدال
ذرة أو مجموعة من الذرات تحل محل جزء من مركب
الاستبدال الأحادي : عنصر واحد يحل محل آخر في مركب
الاستبدال المزدوج : الأيونات السالبة في مركبين تغير من أماكنها
حدد خواص الاحتراق
يطق دائما الأكسجين
غالبا ما ينتج ثاني اكسيد الكربون والماء
مادة متفاعلة دائما الطاقة
حدد نوعين من الطاقة تطلق عادة خلال تفاعلات الاحتراق
الطاقة الحرارية الطاقة الضوئية
لخص الأنواع الأربعة الرئيسية للتفاعلات الكيميائية
تجمع تفاعلات التركيب بين أثنين أو أكثر من العناصر أو المركبات في رمكب واحد ويفكك الانحلال مركب واحد إلى اثنين أو أكثر من المواد وفي تفاعلات الاستبدال يعاد تجميع أجزاء مكونات المركبات لتشكيل مركبات مختلفة ودائما يضمن الاحتراق الأكسجين كمادة متفاعلة ويطلق طاقة
تغيرات الطاقة والتفاعلات الكيميائية
حدد الفرق بين التفاعلات الماصة للحرارة والتفاعلات الطاردة للحرارة
| التفاعل | المواد المتفاعلة +طاقة حرارية تعطي النواتج |
| النوع | ماص للحرارة |
| تغير الطاقة | الطاقة الحرارية الممتصة |
| الروابط التي تضم طاقة أكبر | النواتج |
| التفاعل | المواد المتفاعلة تعطي طاقة حرارية +النواتج |
| النوع | طارد للحرارة |
| تغير الطاقة | الطاقة الحرارية المحررة |
| الروابط التي تضم طاقة أكبر | المتفاعلات |
عرف طاقة التنشيط وحدد أنواع التفاعلات التي تستخدمها
طاقة التنشيط : الحد الأدنى من مقدار الطاقة اللازمة لبدء التفاعل كيميائي
أنواع التفاعلات : ماص للحرارة وطارد للحرارة
سجل عاملين عن التصادمات بين الذرات يؤثران في سرعة التفاعلات الكيميائية
مدى تكرار تصادم الجسيمات
سرعة حركة الجسيمات عند التصادم
اربط بين المساحة السطحية وسرعة التفاعل في المثال التالي
يتفاعل لوح من الطباشير : سرعة التفاعل أبطأ
الشرح : يكون الحمض على تماس فقط مع الجسيمات الواقعة على سطح الطباشير
يتفاعل مسحوق من الطباشير مع الخل :سرعة التفاعل أسرع
الشرح : تكون كمية أكبر من جسيمات الطباشير على تماس مع الحمض
وضح سببين في أن ارتفاع درجة الحرارة يزيد سرعة التفاعل
تزداد السرعة المتوسطة للجسيمات ولذلك تتصادم أكثر
للتصادمات طاقة أكبر وهي أكثر قابلية لكسر الروابط الكيميائية
قارن بين ارتفاع التركيز وارتفاع الضغط على أنهما بمثابة وسيلتين لزيادة سرعة التفاعل
في كلتا الحالتين تكون الجسيمات متقاربة أكثر ما يسبب حدوث تصادمات أكثر فيما بينها
عبر عن العلاقة بين الحفازات والأنزيمات
الأنزيم نوع من الحفازات وهو يسرع التفاعلات الكيميائية داخل الخلايا الحية
قابل بين الحفازات والمثبطات
حفاز : يزيد من سرعة التفاعل عبر تخفيض طاقة التنشيط
مثبط : يبطئ التفاعل الكيميائي أو يوقفه أيضا
الشحنات الكهربائية والقوى الكهربائية
اذكر الفارق بين الجسيمات المحايدة كهربائيا والأجسام المشحونة كهربائيا
محايد كهربائيا : جسيمات بكميات متساوية من الشحنات الموجبة والشحنات السالبة
مشحون كهربائيا : جسم يحتوي على قدرغير متساو من الشحنات الموجبة أو الشحنات السالبة
قارن بين الأجسام موجبة الشحنة وسالبة الشحن
ذات الشحنة الموجبة : جسم اكتسب إلكترونات ويحتوي على إلكترونات أكثر من البروتونات
ذات الشحنة السالبة : جسم تخلى عن الكترونات ويحتوي على بروتونات أكثر من الألكترونات
اذكر تعريف التفريغ الكيميائي
فقدان شحنة كهربائية غير متوازية
سريع : شرارة تظهر بين يدك ومقبض الباب
تدريجي : يختفي الالتصاق الاستاتيكي في الملابس في الايام الرطبة
قارن بين العازلات والموصلات
عازل كهربائي : المادة التي لا تستطيع الشحنات الكهربائية الحركة فيها بسهولة
موصل كهربائي : المادة التي تتحرك فيها الشحنات الكهربائية بسهولة
التيار الكهربائي والدوائر الكهربائية
اربط بين الشحنة الكهربائية بالتيار الكهربائي
التيار الكهربائي هو حركة الجسيمات المشحونة بالكهرباء
قارن بين نوعين من التيار الكهربائي
التيار المستمر : تدفق ثابت للألكترونات في اتجاه واحد
التيار المتناوب : التيار الكهربائي الذي يعكس اللاتجاه باستمرار
ضع تقييما لسمة السلك النحاسي التي تجعله موصلا جيدا للتيار الكهربائي
يتسم النحاس بالمقاومة الكهربائية المنخفضة
ضع تقييما للسبب في أن السلك الخفيف الجيد ينبغي أن يكون قليل المقاومة
ينبغي أن يكون السلك منخفض المقاومة لكي يمنع تبديد الطاقة الكهربائية بتحويلها إلى طاقة حرارية في السلك
حدد مكونا إضافيا مدرجا للأمان أو الراحة في دائرة كهربائية عملية
مفتاح لتشغيل جهاز كهربائي وإيقافه
استنتج السبب في أنه ينبغي ترشيد استهلاك الطاقة الكهربائية
كل العمليات تؤدي إلى التحول من شكل للطاقة إلى طاقة كهربائية تؤثر على البيئة بشكل ما من بين الأمثلة على ذلك التلوث الناتج عن حرق الوقود الأحفوري سيساعد خفض التأثير البشري على البيئة في الحفاظ على حياة أكثر صحة للجميع
الكهرباء والمغناطيسية
اربط بين المغناطيس والمواد المغناطيسية
المغناطيس : جسم يجذب الحديد والمواد الآخرى ذات السمات المغناطيسية المشابهة للحديد
المادة المغناطيسية : أي مادة يجذبها المغناطيس
قارن وقابل بين المجال المغناطيسي ومجال كهربائي
المجال الكهربائي المحيط بجسم مشحون ينتج قوة على الأجسام المشحونة الأخرى المجال المغناطيسي حول مغناطيس ينتج قوة على المغناطيسيات والمواد المغناطيسية الأخرى ينتج المجالان القوى بدون تلامس الأجسام فعليا
صف المغناطيس الكهربائي
مغناطيس مؤقت مصنوع من ملف سلك حامل للتيار ملفوف حول قلب مغناطيسي
استنتج سمة مشتركة بين المواد المغناطيسية والموصلات الكهربائية الجيدة
كلاهما من المعادة في العادة
ميز بين أنواع المغناطيس والمواد المغناطيسية
مادة مغناطيسية ناعمة : تخسر مجالاتها المغناطيسية بسرعة
مادة مغناطيسية صلبة : تحافظ على مجالاتها المغناطيسية لوقت طويل
مغناطيس مؤقت : المادة المغناطيسية التي تتحول إلة مغناطيس عندما يكون في المجال المغناطيسي لمغناطيس دائم
مغناطيس دائم : مادة ذات نطاقات مغناطيسية تظل محتجزة في محاذاة